ADC Linker的关键组成与分类
典型的 ADC 连接子通常由三部分组成:一是用于与抗体连接的生物偶联基团(bioconjugation group),二是控制载荷释放的药物释放触发器(drug release trigger),三是用于调节整体理化性质的间隔基团(spacer)。
图1. 典型的ADC linker结构示意图(图片来自参考文献[1])
根据载荷释放机制,linker可分为两大类:可裂解型(cleavable linker)和不可裂解型(non-cleavable linker)。
可裂解型 linker:包含对肿瘤微环境(Tumor Microenvironment, TME)或细胞内特定条件(如酶、酸性、还原性环境等)敏感的化学键,能在靶细胞内或肿瘤微环境中断裂并释放活性载荷。 不可裂解型 linker:在生理条件下高度稳定,其载荷的释放依赖于抗体在溶酶体内被完全降解。
可裂解Linker的经典设计和前沿进展
这类Linker的设计基于肿瘤细胞内特定酶(尤其是溶酶体中的组织蛋白酶B,Cathepsin B)的高表达特性,能够实现肿瘤特异性的药物释放。
经典设计:最具代表性的酶敏感linker是缬氨酸-瓜氨酸(Val-Cit)二肽结构,可被组织蛋白酶B高效识别并切割。该结构常与自降解间隔基PABC联用,在酶切后触发PABC自发分解,以“无痕”方式释放完整活性药物(如MMAE(monomethyl auristatin E))。这一策略已在多款已获批ADC药物中得到成功应用,如维布妥昔单抗(Brentuximab vedotin)。
前沿进展:尽管Val-Cit应用广泛,但其在小鼠模型中表现出血浆稳定性不足的问题,限制了临床前评价的准确性。为此,研究人员开发了更稳定的三肽linker,例如EVCit(谷氨酸-缬氨酸-瓜氨酸)与EGCit(谷氨酸-甘氨酸-瓜氨酸),它们显著延长了血浆半衰期,有望带来更宽的治疗窗口。
2. 酸裂解型linker
该类linker利用肿瘤微环境及细胞内内涵体/溶酶体的酸性条件实现药物释放,具有良好的肿瘤区域选择性。
经典设计:常用的酸敏感基团包括腙键与碳酸酯键。例如,首款获批ADC药物吉妥珠单抗(Gemtuzumab ozogamicin)使用了含腙键的AcBut(4-(4-acetyl-phenoxy)-butyric acid) linker;而戈沙妥珠单抗(Sacituzumab govitecan)则采用CL2A linker,其碳酸酯结构在酸性条件下水解,释放SN-38载荷。 前沿进展:近年来,更多新型酸响应化学键被开发出来,如甲硅烷基醚及源自天然产物没食子酸的交联结构。这些创新结构展现出更快的酸响应速率与可调的稳定性,为下一代酸敏感linker设计提供了多样化选择。
经典设计:二硫键是目前最常用的还原敏感基团,其在循环系统中稳定,进入细胞后被高浓度GSH还原断裂。代表性药物索米妥昔单抗(Mirvetuximab soravtansine),即采用基于二硫键的Sulfo-SPDB linker实现有效载荷定向释放。 前沿进展:为提高二硫键的血浆稳定性,当前策略主要围绕在其邻位引入空间位阻基团。此外,二硒键作为一种新型“双重响应”结构,可同时响应GSH与活性氧,展现出良好的应用前景。
生物偶联基团和间隔基团的优化策略
引入亲水基团:通过在间隔基团中嵌入亲水单元,有效降低ADC分子的聚集倾向,改善制剂的长期稳定性。 构建分支结构:开发分支型linker,使其能够同时搭载不同机制的药物,如细胞毒药物与免疫调节剂,实现协同载荷的共同递送,从而提升疗效或克服耐药性。
RCS一站式ADC Linker-Payload平台
可靠:拥有超过10年的ADC领域经验,已成功交付超过27,000个相关化合物。 多样:化合物库拥有1000多种linker,覆盖30多种连接位点和新颖载荷,形成了完善的“模块化”体系,可快速设计和组合,满足多样化的定制需求。 灵活:支持从毫克到百克级的规模化合成,提供FTE(Full-time Equivalent)或FFS(Fee-for-Service)等多种灵活的合作模式。 全方位支持:配备高效的分离纯化平台、完备的分析支持(LC-MS, NMR等)以及高活实验室,确保对高活性、高难度分子的安全处理和高质量交付。 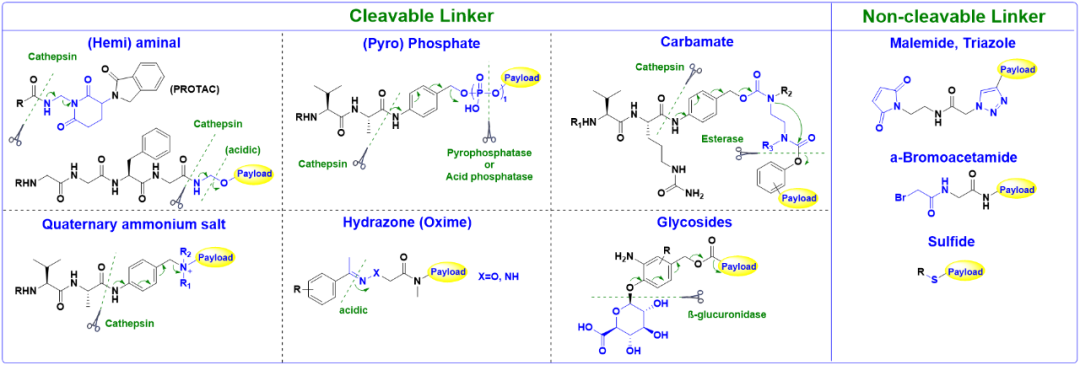
参考文献: 1. Linker Design for The Antibody Drug Conjugates: A Comprehensive Review,ChemMedChem 2025, e202500262 免责声明:本文章仅供讨论和参考,不构成提供所述化合物或技术的许诺销售。我司将对客户订单进行全面的法律风险评估,在确认未侵犯第三方知识产权的情况下,方会提供相关服务。 










